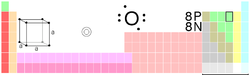
Oksygen
| |||||||||||||||||||||||||||||||
Generelle eigenskapar | |||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
Namn, kjemisk symbol, atomnummer | Oksygen, O, 8 | ||||||||||||||||||||||||||||||
Kjemisk serie | Ikkje-metall | ||||||||||||||||||||||||||||||
Gruppe, periode, blokk | 16, 2, p | ||||||||||||||||||||||||||||||
Tettleik, hardleik | 1,429 kg/m3, n.a. (ikkje SI) | ||||||||||||||||||||||||||||||
Utsjånad | Fargelaus  | ||||||||||||||||||||||||||||||
Atomeigenskapar | |||||||||||||||||||||||||||||||
Atommasse | 15,9994 u (ikkje SI) | ||||||||||||||||||||||||||||||
Atomradius (berekna) | 60 (48) pm | ||||||||||||||||||||||||||||||
Kovalent radius | 73 pm | ||||||||||||||||||||||||||||||
Ioneradius | 140 pm (ladning: −2) | ||||||||||||||||||||||||||||||
van der Waals radius | 152 pm | ||||||||||||||||||||||||||||||
Elektronkonfigurasjon | [He]2s22p4 | ||||||||||||||||||||||||||||||
Elektron per energinivå | 2, 6 | ||||||||||||||||||||||||||||||
Oksidasjonstrinn (oksid) | −2, −1 (nøytralt) | ||||||||||||||||||||||||||||||
Krystallstruktur | Kubisk | ||||||||||||||||||||||||||||||
Fysiske eigenskapar | |||||||||||||||||||||||||||||||
Tilstandsform | Gass | ||||||||||||||||||||||||||||||
Smeltepunkt | 50,35 K (−222,8°C) | ||||||||||||||||||||||||||||||
Kokepunkt | 90,18 K (−182,97°C) | ||||||||||||||||||||||||||||||
Molart volum | 11200 cm3/mol | ||||||||||||||||||||||||||||||
Fordampingsvarme | 3,4099 kJ/mol | ||||||||||||||||||||||||||||||
Smeltevarme | 0,22259 kJ/mol | ||||||||||||||||||||||||||||||
Damptrykk | (?) Pa ved K | ||||||||||||||||||||||||||||||
Ljodfart | 317,5 m/s ved 25 °C | ||||||||||||||||||||||||||||||
Diverse eigenskapar | |||||||||||||||||||||||||||||||
Elektronegativitet | 3,44 (Paulings skala) | ||||||||||||||||||||||||||||||
Spesifikk varmekapasitet | 920 J/(kg·K) | ||||||||||||||||||||||||||||||
Elektrisk konduktivitet | (?) MS/m | ||||||||||||||||||||||||||||||
Termisk konduktivitet | 0,02674 W/(m·K) | ||||||||||||||||||||||||||||||
Ioniseringspotensial | 1320 kJ/mol 3395 kJ/mol 5307 kJ/mol 7476 kJ/mol 10996 kJ/mol 13333 kJ/mol 71343 kJ/mol 84086 kJ/mol | ||||||||||||||||||||||||||||||
Mest stabile isotopar | |||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
SI-einingar og STP er brukt unntatt der det er avmerkt | |||||||||||||||||||||||||||||||
Oksygen, eldre òg surstoff eller nøre, er eit grunnstoff med kjemisk symbol O og atomnummer 8. Det høyrer til ikkje-metalla, og ligg i gruppe 16 i det periodiske systemet. Grunnstoffet har to allotrope former, oksygengass (O2) og ozon (O3). Oksygenmolekylet er vanlegvis paramagnetisk, men diamagnetisk former finst.
Innhaldsliste
1 Særlege kjenneteikn
2 Bruk
3 Historie
4 Biologisk rolle
5 Førekomst og framstilling
6 Kjemi og sambindingar
7 Isotopar
8 Tryggleik
9 Sjå òg
10 Kjelder
Særlege kjenneteikn |
Oksygen er elektronegativt. Som dioksygen, O2, er oksygen ein fargelaus, luktfri gass. I væskeform er stoffet svakt blåfarga. Molekylet er ikkje polart. Oksygengass er lite løyseleg i vatn.
Ozon er ein termodynamisk ustabil diamagnetisk gass med sterk lukt.
Bruk |
Historie |
Oksygen vart oppdaga på 1700-talet. Joseph Priestley, Carl Wilhelm Scheele og Antoine Lavoisier var med på dette.
Biologisk rolle |
Oksygengass vert danna under fotosyntesen, og er viktig for dyr og menneske.
Førekomst og framstilling |
Oksygen er det vanlegaste grunnstoffa på jorda. Jordatmosfæren inneheld om lag 21 % oksygengass og nesten halvparten av alle atom i jordskorpa er oksygenatom. I jordskorpa finst grunnstoffet særleg som SiO2. I tillegg finst store mengder bundne i vatn (H2O). Mange syrer og basar inneheld oksygen.
Oksygen vert vanlegvis framstilt ved fraksjonell destillering av luft. I laboratoriet er det mogleg å framstilla gassen på fleire måtar.
Kjemi og sambindingar |
Sidan oksygenatomet er lite og dannar sterke dobbeltbindingar, får det ikkje meir enn fire kovalente bindingar.
Nesten alle grunnstoff reagerer med O2-molekylet anten ved romtemperatur eller ved oppvarming. Det er derfor ein viktig reagens.
Oksygen er med i mange sambindingar, både organiske og uorganiske. Alkoholar, aldehyd og karboksylsyrer er eksempel på organiske sambindingar. Elles er oksygen mellom anna med i oksid (til dømes karbondioksid (CO2), Hydrogenperoksid (H2O2) og vatn (H2O).
Oksid kan vera sure, basiske eller amfotære avhengig av kva andre grunnstoff dei inneheld.
Isotopar |
Tryggleik |
Ozon er giftig.
Sjå òg |
- Chalkogen
- Ozonlaget
Kjelder |
- Geoff Rayner-Canham: Descriptive Inorganic Chemistry 2.ed. New York, 2000
Webelements - informasjon om oksygen på engelsk
 Denne kjemiartikkelen er ei spire. Du kan hjelpe Nynorsk Wikipedia gjennom å utvide han.
Denne kjemiartikkelen er ei spire. Du kan hjelpe Nynorsk Wikipedia gjennom å utvide han.
|